1. Loét tiêu hóa do thuốc kháng kết tập tiểu cầu: cơ chế và yếu tố thúc đẩy
1.1. Đại cương về nhóm thuốc kháng kết tập tiểu cầu
Thuốc kháng kết tập tiểu cầu (antiplatelet drugs) là nhóm thuốc nền tảng trong điều trị và phòng ngừa thứ phát các bệnh lý tim mạch do huyết khối động mạch. Các thuốc này can thiệp vào các giai đoạn khác nhau của quá trình hoạt hóa và kết dính tiểu cầu, từ đó ngăn chặn tiểu cầu vón cục tạo thành cục máu đông gây tắc nghẽn lòng mạch. Dựa vào cơ chế tác động, thuốc kháng kết tập tiểu cầu được chia thành các nhóm chính sau:
- Thuốc ức chế không hồi phục Cyclooxygenase-1 (COX-1): Aspirin ngăn chặn sự tổng hợp thromboxane A2 (TXA2) – một chất gây co mạch và kích hoạt tiểu cầu mạnh mẽ.
- Thuốc ức chế thụ thể P2Y12: Gồm các thuốc đường uống như Clopidogrel, Prasugrel, Ticagrelor … Các thuốc này gắn vào và phong bế thụ thể P2Y12 trên màng tiểu cầu, ngăn chặn sự hoạt hóa tiểu cầu do phân tử adenosine diphosphate (ADP) làm trung gian.
- Một số nhóm khác như thuốc đối kháng thụ thể Glycoprotein (GP) IIb/IIIa (abciximab, eptifibatid và tirofiban) và nhóm ức chế Phosphodiesterase (cilostazol hoặc dipyridamol).
Thuốc kháng kết tập tiểu cầu được chỉ định rộng rãi trong thực hành tim mạch và thần kinh, bao gồm: Hội chứng mạch vành cấp (ACS), Hội chứng mạch vành mạn (CCS); dự phòng biến cố tim mạch thứ phát sau can thiệp mạch vành qua da (PCI); dự phòng đột quỵ và thuyên tắc huyết khối ở bệnh nhân có tiền sử đột quỵ thiếu máu não, TIA, hoặc bệnh lý động mạch ngoại biên…
Liệu pháp kháng kết tập tiểu cầu kép (dual antiplatelet therapy, DAPT) là sự kết hợp đồng thời của hai loại thuốc kháng kết tập tiểu cầu có cơ chế tác dụng khác nhau, bao gồm aspirin liều thấp và thuốc ức chế P2Y12. Sự ức chế kép này tạo ra hiệu ứng hiệp lực, giúp giảm mạnh nguy cơ hình thành huyết khối tại vị trí tổn thương nội mạc mạch máu hiệu quả hơn nhiều so với việc chỉ dùng một loại thuốc. Đây là một chiến lược điều trị nền tảng trong chuyên ngành tim mạch và thần kinh, nhằm tối ưu hóa việc phòng ngừa sự hình thành cục máu đông.
1.2. Xuất huyết tiêu hóa liên quan đến thuốc kháng kết tập tiểu cầu
1.2.1. Đại cương về biến cố xuất huyết do thuốc kháng kết tập tiểu cầu
Xuất huyết là tác dụng phụ điển hình và quan trọng nhất cần chú ý khi sử dụng thuốc ức chế kết tập tiểu cầu, bao gồm xuất huyết tiêu hóa, xuất huyết nội sọ, bầm tím dưới da, và chảy máu tại các vị trí phẫu thuật.
Trong số các biến chứng xuất huyết do thuốc kháng kết tập tiểu cầu gây ra, xuất huyết tiêu hóa (XHTH) là một trong những loại xuất huyết nghiêm trọng thường gặp nhất ở những người dùng thuốc kháng tiểu cầu và có khả năng gây tử vong. Nhìn chung, XHTH do thuốc kháng tiểu cầu được xếp vào nhóm các biến cố bất lợi do thuốc thường gặp nhất trong thực tế lâm sàng. Nguy cơ tăng vọt khi sử dụng liệu pháp kép (DAPT).
Sự nguy hiểm của XHTH không chỉ nằm ở tình trạng mất máu cấp tính có thể đe dọa tính mạng (gây sốc giảm thể tích), mà còn ở chỗ biến cố này buộc bác sĩ và bệnh nhân phải ngừng sử dụng thuốc kháng kết tập tiểu cầu. Việc ngưng thuốc (đặc biệt là DAPT) được xác định là một yếu tố nguy cơ độc lập dẫn đến tiên lượng lâm sàng rất kém. Khi ngưng thuốc để cầm máu dạ dày, bệnh nhân đối mặt với nguy cơ khôi phục lại tình trạng kết tập tiểu cầu, dẫn đến những hậu quả tai hại trong trung và dài hạn như nhồi máu cơ tim tái phát, huyết khối trong stent và tử vong do nguyên nhân tim mạch.
1.2.2. Cơ chế về biến cố xuất huyết do thuốc kháng kết tập tiểu cầu
Cơ chế gây xuất huyết tiêu hóa của thuốc kháng kết tập tiểu cầu là sự kết hợp giữa việc phá vỡ hàng rào bảo vệ sinh lý tự nhiên của dạ dày và làm suy yếu cơ chế cầm máu – khắc phục các tổn thương ở cấp độ phân tử. Cơ chế này có sự khác biệt rõ rệt giữa Aspirin và các thuốc ức chế thụ thể P2Y12 (như Clopidogrel, Prasugrel, Ticagrelor), cụ thể như sau
Cơ chế của Aspirin: Gây tổn thương trực tiếp hàng rào bảo vệ niêm mạc dạ dày
- Ở cấp độ phân tử: aspirin ức chế không hồi phục enzyme cyclooxygenase-1 (COX-1), qua đó ngăn chặn quá trình chuyển hóa acid arachidonic thành thromboxane A2 (TXA2) và các prostaglandin (như PGE2 ).
- Ở cấp độ sinh lý: PGE2 đóng vai trò chủ yếu trong việc duy trì hàng rào bảo vệ niêm mạc dạ dày bằng cách tăng cường lưu lượng máu đến niêm mạc, kích thích sự phân bào của tế bào biểu mô, thúc đẩy tiết chất nhầy cùng bicarbonate để trung hòa acid. Khi quá trình tổng hợp PGE2 bị ức chế bởi aspirin, hàng rào bảo vệ này suy yếu nghiêm trọng. Sự sụt giảm tiết chất nhầy và bicarbonate khiến niêm mạc dạ dày trở nên nhạy cảm và dễ bị tổn thương, ăn mòn bởi các yếu tố tấn công nội sinh như acid dạ dày, enzyme pepsin và muối mật.
Cơ chế của nhóm ức chế P2Y12: Khác với Aspirin, Clopidogrel (và các thuốc P2Y12 khác) không trực tiếp gây tổn thương hay loét niêm mạc dạ dày. Cơ chế gây chảy máu của nhóm này diễn ra một cách gián tiếp và mang tính toàn thân:
- Ở cấp độ phân tử: Clopidogrel (ở dạng hoạt động) gắn không hồi phục vào thụ thể P2Y12 trên màng tiểu cầu, ngăn không cho phân tử ADP gắn vào, từ đó chặn đứng tín hiệu hoạt hóa tiểu cầu
- Ở mức độ sinh lý: ức chế tiên phát cầm máu ban đầu và cản trở tiên trình phục hồi cac tổn thương
+ Ức chế tiên phát quá trình cầm máu ban đầu: Khi niêm mạc dạ dày xuất hiện các vết xước hoặc vết loét nhỏ (do acid, dùng chung NSAIDs, hoặc nhiễm vi khuẩn Helicobacter pylori), tiểu cầu không thể kết tập để tạo thành nút cầm máu tại vị trí tổn thương mạch máu.
+ Cản trở quá trình phục hồi: Bình thường, tiểu cầu hoạt hóa tại vết thương sẽ giải phóng ra các yếu tố tăng trưởng giúp làm lành mô. Thuốc kháng kết tập tiểu cầu ức chế quá trình này, làm giảm sự giải phóng yếu tố tăng trưởng. Ngoài ra, clopidogrel còn có tác dụng ức chế tân tạo mạch máu. Hậu quả là thuốc làm chậm, cản trở hoặc làm mất khả năng tự chữa lành của các vết xước và loét niêm mạc hiện có, khiến những tổn thương nhỏ này dễ dàng tiến triển thành các biến cố xuất huyết lớn.
Khi dùng liệu pháp kháng tiểu cầu kép (DAPT), cơ chế gây xuất huyết bị khuếch đại do
- Aspirin “mở đường” bằng cách ức chế COX-1, làm suy giảm hàng rào bảo vệ, tạo ra các vết loét và trợt niêm mạc dạ dày.
- Clopidogrel/Prasugrel/Ticagrelor “ngăn chặn phục hồi” bằng cách ức chế hệ thống tiểu cầu toàn thân, khiến các vết loét do aspirin tạo ra không thể tự cầm máu và không thể lành lại.
1.3. Một số yếu tố thúc đẩy xuất huyết ở người dùng thuốc kháng kết tập tiểu cầu
Trên lâm sàng, nhiều yếu tố khác nhau có thể thúc đẩy và làm gia tăng nguy cơ xuất huyết tiêu hóa (XHTH) trên bệnh nhân sử dụng thuốc kháng kết tập tiểu cầu. Các yếu tố này có thể được phân loại thành hai nhóm chính:
1.3.1. Nhóm các yếu tố không thay đổi được
Đây là các yếu tố mang tính cố hữu của người bệnh, giúp bác sĩ, dược sĩ nhận diện bệnh nhân thuộc nhóm nguy cơ cao ngay từ khi tiếp cận:
- Tuổi cao: Tuổi càng cao, nguy cơ xuất huyết càng lớn
- Giới tính: Nữ giới có nguy cơ xuất huyết cao hơn
- Tiền sử bệnh lý tiêu hóa: từng bị xuất huyết tiêu hóa trước đó hoặc có tiền sử loét dạ dày - tá tràng.
- Bệnh lý cơ quan mạn tính như
+ Suy thận mạn tính: Suy giảm chức năng thận làm suy yếu chức năng tiểu cầu nội sinh và tăng nguy cơ chảy máu.
+ Bệnh gan mạn tính: Suy gan, xơ gan, đặc biệt là xơ gan có tăng áp lực tĩnh mạch cửa.
+ Bệnh lý huyết học và ung thư: Tình trạng giảm tiểu cầu mức độ trung bình đến nặng (< 100 x 109/L), rối loạn đông cầm máu cơ bản, tình trạng thiếu máu, hoặc đang mắc các bệnh lý ung thư (ác tính) đang hoạt động.
+ Bệnh lý thần kinh: từng bị đột quỵ, xuất huyết nội sọ hoặc dị dạng động tĩnh mạch não.
- Yếu tố di truyền: Các đa hình gen ảnh hưởng đến chuyển hóa thuốc kháng tiểu cầu. nếu một bệnh nhân mang biến thể gen CYP2C19*17, cơ thể sẽ chuyển hóa clopidogrel quá mạnh mẽ, dẫn đến mức độ ức chế tiểu cầu vượt quá ranh giới an toàn sinh lý và đối mặt với nguy cơ xuất huyết (như xuất huyết tiêu hóa, xuất huyết nội sọ) cao hơn
1.3.2. Nhóm các yếu tố có thể thay đổi được
Đây là các yếu tố mà bác sĩ, dược sĩ và bệnh nhân có thể chủ động điều chỉnh để giảm thiểu nguy cơ xuất huyết:
- Phối hợp nhiều loại thuốc có nguy cơ xuất huyết cao:
+ Sử dụng liệu pháp kháng tiểu cầu kép (DAPT) (kết hợp aspirin và một thuốc P2Y12 như clopidogrel), hoặc dùng aspirin liều cao. Nguy cơ XHTH cũng tăng lên nếu dùng DAPT kéo dài (trên 6 tháng).
- Dùng đồng thời với các thuốc chống đông máu (như kháng vitamin K - VKA, hoặc thuốc chống đông đường uống thế hệ mới - DOAC).
- Dùng đồng thời với các thuốc kháng viêm không steroid (NSAIDs), thuốc ức chế chọn lọ COX-2, hoặc corticosteroid (steroid).
- Các bệnh lý dạ dày - tá tràng hiện mắc:
+ Tình trạng nhiễm vi khuẩn Helicobacter pylori chưa được diệt trừ (yếu tố này làm tăng gấp đôi nguy cơ XHTH).
+ Có các triệu chứng khó tiêu hoặc bệnh trào ngược dạ dày thực quản (GERD).
- Lối sống và các bệnh lý toàn thân có thể kiểm soát:
+ Thói quen hút thuốc lá và sử dụng rượu mạn tính.
+ Tình trạng béo phì hoặc bệnh tăng huyết áp chưa được kiểm soát tốt.
2. Dự phòng xuất huyết tiêu hóa do thuốc kháng kết tập tiểu cầu bằng thuốc ức chế bơm proton: lợi ích và nguy cơ
2.1. Cơ chế bảo vệ dạ dày của thuốc ức chế bơm proton
Cơ chế bảo vệ dạ dày và dự phòng xuất huyết tiêu hóa của thuốc ức chế bơm proton (PPI) chủ yếu dựa trên khả năng ức chế kéo dài quá trình tiết acid dịch vị, từ đó loại bỏ yếu tố tấn công chính lên lớp niêm mạc đang bị suy yếu do thuốc kháng kết tập tiểu cầu. Mặc dù thời gian bán thải trong máu của PPI rất ngắn (chỉ 1-2 giờ), nhưng do chúng gắn kết không hồi phục với bơm proton, tế bào thành dạ dày buộc phải tổng hợp các bơm proton mới để có thể khôi phục lại khả năng tiết acid (khoảng 36 giờ).
2.2. Lợi ích dự phòng xuất huyết tiêu hóa ở bệnh nhân sử dụng thuốc ức chế kết tập tiểu cầu bằng thuốc ức chế bơm proton
Bằng chứng từ các thử nghiệm lâm sàng ngẫu nhiên có đối chứng (RCT) và các phân tích gộp (systematic review/meta-analysis) đã khẳng định rõ ràng lợi ích vượt trội của PPI trong việc dự phòng XHTH trên bệnh nhân sử dụng thuốc kháng kết tập tiểu cầu.
2.2.1. Đối với nhóm dùng liệu pháp kháng kết tập tiểu cầu kép (DAPT)
Những bệnh nhân sử dụng DAPT là nhóm có nguy cơ XHTH rất cao, và bằng chứng ủng hộ việc dùng PPI ở nhóm này là mạnh mẽ nhất:
- Thử nghiệm COGENT (RCT lớn nhất): thử nghiệm ngẫu nhiên mù đôi đa trung tâm, tiến hành trên 3.761 bệnh nhân có chỉ định dùng DAPT (aspirin + clopidogrel) do hội chứng vành cấp hoặc đặt stent. Bệnh nhân được chia ngẫu nhiên dùng kèm omeprazole hoặc giả dược. Kết quả cho thấy nhóm dùng omeprazole giúp giảm tới 66% các biến cố tiêu hóa, bao gồm XHTH (1,1% ở nhóm dùng omeprazole so với 2,9% ở nhóm giả dược, HR = 0,34; p < 0,001). Một phân tích gộp cập nhật (2025) sử dụng dữ liệu từ COGENT cho thấy PPI làm giảm tổng nguy cơ XHTH (RR = 0,22) nhưng không làm tăng các biến cố tim mạch.
- Một phân tích gộp của Luo và cộng sự (2023) phân tích trên 173.508 bệnh nhân từ 18 nghiên cứu (gồm RCT và thuần tập) dùng DAPT. Kết quả cho thấy việc sử dụng đồng thời PPI giúp giảm 56% nguy cơ biến cố tiêu hóa (HR = 0,44, 95% CI: 0,30–0,64, p < 0,0001).
2.2.2. Nhóm bệnh nhân sử dụng Clopidogrel đơn trị liệu
Khi đánh giá về hiệu quả và tính an toàn của clopidogrel khi dùng kèm hoặc không kèm PPI, phần lớn các nghiên cứu RCT hiện nay gợi ý rằng việc sử dụng đồng thời PPI với clopidogrel có khả năng làm giảm nguy cơ xuất huyết tiêu hóa rõ rệt.
Tuy nhiên, việc sử dụng PPI dự phòng không mang lại lợi ích rõ rệt cho tất cả mọi bệnh nhân dùng thuốc kháng kết tập tiểu cầu, mà chỉ thể hiện lợi ích vượt trội trên nhóm có nguy cơ cao XHTH. Tỷ lệ nền (baseline risk) của biến cố XHTH ở những bệnh nhân không có yếu tố nguy cơ vốn đã rất thấp. Khi sử dụng PPI cho nhóm bệnh nhân nguy cơ thấp, lợi ích mang lại có thế rất thấp. Cụ thể, theo một nghiên cứu quy mô lớn trên 46.301 bệnh nhân, tỷ lệ XHTH sau 1 năm ở nhóm nguy cơ thấp chỉ là 1,0%, so với 1,7% ở nhóm nguy cơ cao. Cần chú ý, việc dùng PPI giúp giảm nguy cơ tuyệt đối rất nhỏ, chỉ khoảng 0,44% ở nhóm nguy cơ thấp. Vì nguy cơ chảy máu ban đầu thấp, bác sĩ sẽ phải kê đơn PPI cho một số lượng rất lớn bệnh nhân mới có thể ngăn ngừa được 1 ca XHTH, dẫn đến việc sử dụng thường quy (cho mọi bệnh nhân) trở nên lãng phí và không đem lại hiệu quả lâm sàng rõ rệt trên diện rộng. Do vậy cần đánh giá bệnh nhân để cá thể hóa trong quyết định dự phòng bằng PPI khi BN có sử dụng thuốc kháng kết tập tiểu cầu dựa trên các yếu tô nguy cơ kèm theo (mục 1.3.2).
2.3. Nguy cơ và ý nghĩa lâm sàng của tương tác thuốc bất lợi giữa thuốc ức chế kết tập tiểu cầu và thuốc ức chế bơm proton
2.3.1. Cơ chế tương tác giữa PPI và thuốc kháng kết tập tiểu cầu
Bản chất clopidogrel là một tiền chất không có hoạt tính dược lý. Sau khi được uống và hấp thu (chỉ khoảng 15% lượng thuốc đi vào gan), clopidogrel chuyển hóa tại gan bởi CYP2C19 để trở thành dạng chất chuyển hóa có hoạt tính. Chất chuyển hóa có hoạt tính này mới có khả năng gắn không hồi phục vào thụ thể P2Y12 trên màng tiểu cầu, từ đó phát huy tác dụng ức chế kết tập tiểu cầu.
Phần lớn các thuốc nhóm PPI cũng được chuyển hóa mạnh tại gan bởi hệ enzym cytochrome P450, chủ yếu thông qua con đường CYP2C19 và một phần qua CYP3A4. Bên cạnh việc là cơ chất cần được chuyển hóa, các PPI đồng thời đóng vai trò là chất ức chế cạnh tranh đối với chính enzym CYP2C19.
Khi bệnh nhân sử dụng đồng thời, PPI sẽ cạnh tranh với clopidogrel tại vị trí xúc tác của enzym CYP2C19. Do CYP2C19 bị PPI chiếm giữ hoặc ức chế, quá trình chuyển hóa tiền chất clopidogrel bị cản trở. Kết quả co nguy cơ làm giảm đáng kể lượng chất chuyển hóa có hoạt tính của clopidogrel được tạo ra trong máu. Điều này có thể làm suy giảm hiệu lực ức chế kết tập tiểu cầu, khiến bệnh nhân không được bảo vệ đầy đủ và đối mặt với nguy cơ gia tăng các biến cố huyết khối tim mạch (như tái nhồi máu cơ tim, huyết khối trong stent).
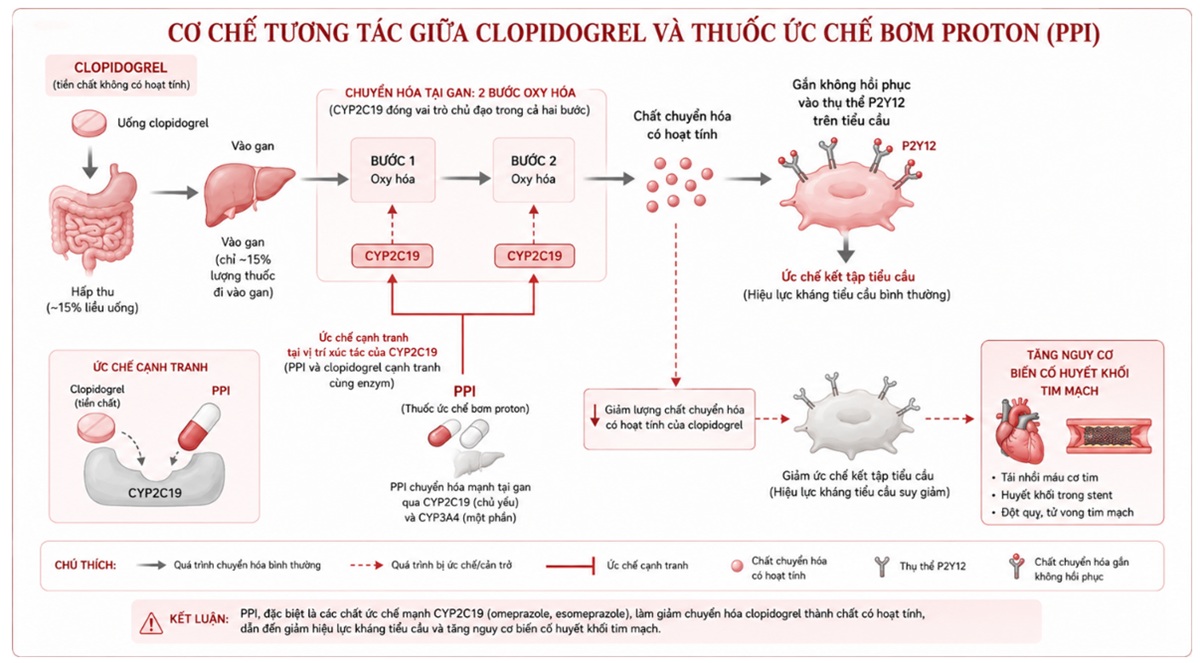
Hình 3.1. Cơ chế tương tác giữa clopidogrel và thuốức chế bơm proton
Mức độ tương tác có thể khác nhau giữa các thế hệ PPI: Khả năng ức chế CYP2C19 không đồng đều giữa các loại thuốc trong nhóm PPI, do đó mức độ tương tác làm giảm hiệu lực của clopidogrel cũng có sự khác biệt. Nguy cơ cao nhất được dự đoán có thể gặp khi dùng omeprazol và Esomeprazol vì đây là những chất ức chế mạnh enzym CYP2C19. Lansoprazole ức chế CYP2C19 ở mức độ vừa phải. Nguy cơ thấp nhất được dự đoán khi dùng pantoprazol và Rabeprazol vì pantoprazole là chất ức chế rất yếu đối với CYP2C19 và được chuyển hóa thêm qua con đường khác (như sulfotransferase). Trong khi đó, rabeprazole chủ yếu bị phân hủy qua con đường không liên quan đến enzym (non-enzymatic). Do đó, về mặt dược lý lâm sàng, pantoprazol hoặc rabeprazole là những lựa chọn được ưu tiên khi bệnh nhân bắt buộc phải dùng PPI chung với clopidogrel để bảo vệ dạ dày.
2.3.2. Ý nghĩa lâm sàng của tương tác giữa PPI và thuốc kháng kết tập tiểu cầu trên các nhóm đối tượng có nguy cơ tim mạch khác nhau
Mặc dù về mặt dược lý cho thấy PPI (đặc biệt là omeprazol) ức chế enzym CYP2C19 làm giảm tác dụng kháng tiểu cầu của clopidogrel, việc tương tác này có dẫn đến hậu quả lâm sàng hay không vẫn còn nhiều tranh cãi.
Ý nghĩa lâm sàng của tương tác giữa thuốc ức chế bơm proton (PPI) và thuốc kháng kết tập tiểu cầu (đặc biệt là clopidogrel) là một vấn đề phức tạp, còn nhiều tranh cải, phụ thuộc rất lớn vào việc đánh giá cán cân giữa nguy cơ huyết khối tim mạch và nguy cơ xuất huyết tiêu hóa (XHTH) của từng bệnh nhân.
Sự gia tăng nguy cơ biến cố tim mạch chính (MACE) chủ yếu được ghi nhận trong các nghiên cứu quan sát. Khi phân tích dữ liệu từ các RCT hoặc các nghiên cứu có điều chỉnh xu hướng, nguy cơ MACE gia tăng thường không có ý nghĩa. Điều này gợi ý rằng việc sử dụng PPI có thể chỉ là một dự báo của bệnh nhân có nhiều bệnh lý nền nặng hơn (tuổi cao, nhiều bệnh đồng mắc) chứ không phải là nguyên nhân trực tiếp gây ra MACE.
- Nhóm bệnh nhân sau can thiệp mạch vành qua da (PCI) / Đặt stent
Đây là nhóm có nguy cơ tái nhồi máu cơ tim và huyết khối trong stent cao nhất nếu tác dụng của clopidogrel bị suy giảm.
Ý nghĩa lâm sàng: Một phân tích gộp thực hiện riêng trên nhóm bệnh nhân PCI (50.277 bệnh nhân) cho thấy việc dùng đồng thời clopidogrel và PPI liên quan đến sự gia tăng có ý nghĩa thống kê về nguy cơ MACE, nhồi máu cơ tim và đột quỵ so với dùng clopidogrel đơn độc. Tuy nhiên, một số nghiên cứu khác cho rằng sự gia tăng MACE ở nhóm này cũng có thể do các yếu tố nhiễu như đặc điểm tổn thương mạch vành phức tạp mà không chắc chắn do tương tác thuốc.
Định hướng xử trí: Nếu có thể, tránh khởi trị PPI ở nhóm này. Nếu bệnh nhân bắt buộc phải dùng liệu pháp kháng tiểu cầu kép (DAPT), việc dự phòng bằng PPI để tránh xuất huyết có thể cần thiết và nếu bắt buộc dùng PPI, ưu tiên các PPI ít chuyển hóa qua CYP2C19 như pantoprazol và rabeprazol.
- Nhóm bệnh nhân Hội chứng vành cấp (ACS) điều trị nội khoa hoặc bệnh mạch vành mạn, bệnh nhân đột quỵ thiếu máu não hoặc TIA
Đây là những bệnh nhân cần dùng DAPT hoặc đơn trị liệu để dự phòng thứ phát, nguy cơ huyết khối thấp hơn nhóm vừa can thiệp PCI.
Ý nghĩa lâm sàng: Các RCT (như COGENT) và nhiều phân tích gộp cho thấy trên nhóm đối tượng này, lợi ích giảm XHTH của PPI là rất rõ rệt và vượt trội hơn nguy cơ gia tăng MACE. XHTH trong quá trình dùng kháng tiểu cầu là một biến chứng nguy hiểm, có thể dẫn đến buộc ngưng sử dụng DAPT nếu xảy ra, do đó có liên quan đến gia tăng tử vong do mọi nguyên nhân.
Định hướng xử trí: Cân nhắc kỹ lợi ích/nguy cơ. Nếu bệnh nhân có nguy cơ tiêu hóa cao, việc kê đơn PPI là bắt buộc và ưu tiên pantoprazol, rabeprazol.
- Nhóm sử dụng clopidogrel đơn trị
Đặc điểm: Những bệnh nhân dùng clopidogrel đơn trị để dự phòng tiên phát các biến cố tim mạch trong hội chứng mạch vành mạn.
Ý nghĩa lâm sàng: Ở bệnh nhân có nguy cơ XHTH thấp, việc sử dụng PPI dự phòng thường quy mang lại lợi ích rất nhỏ, không đáng kể, trong khi lại khiến bệnh nhân phải đối mặt với nguy cơ tương tác thuốc làm giảm hiệu quả bảo vệ tim mạch cũng như các tác dụng phụ dài hạn của PPI.
Định hướng xử trí: Không khuyến cáo sử dụng PPI thường quy trừ khi bệnh nhân có nguy cơ XHTH cao do bệnh lý đồng mắc hoặc đang dùng cùng NSAIDs.
2.4. Một số gợi ý các bước cá thể hóa trong quản lý xuất huyết tiêu hóa ở bệnh nhân sử dụng thuốc ức chế kết tập tiểu cầu bằng thuốc ức chế bơm proton
Dựa trên phân tầng nguy cơ của bệnh nhân, các hướng dẫn lâm sàng (ACC/AHA, ESC) định hướng các bước xử trí như sau:
Bước 1: Chỉ khuyến cáo sử dụng PPI khi bệnh nhân có nguy cơ XHTH cao. Không dùng PPI thường quy như một thuốc “đi cùng” clopidogrel. PPI chỉ được cân nhắc chỉ định kết hợp với thuốc kháng tiểu cầu ở những bệnh nhân có yếu tố nguy cơ XHTH như:
- Đang điều trị bằng liệu pháp DAPT
- Tiền sử loét dạ dày - tá tràng hoặc từng bị XHTH.
- Tuổi cao (trên 65 tuổi).
- Dùng đồng thời với thuốc chống đông máu, thuốc kháng viêm không steroid (NSAID), hoặc corticosteroid.
- Nhiễm Helicobacter pylori.
Bước 2: Lựa chọn PPI an toàn về mặt dược lý nếu bệnh nhân dùng clopidogrel và bắt buộc phải dùng PPI:
- Nên tránh kê đơn omeprazol và esomeprazol do đây là các chất ức chế mạnh CYP2C19, làm giảm hiệu quả của clopidogrel.
- Ưu tiên lựa chọn pantoprazole hoặc rabeprazole: Hai PPI này ít bị chuyển hóa bởi CYP2C19 hoặc là chất ức chế rất yếu, do đó có nguy cơ tương tác thuốc thấp nhất và an toàn hơn cho tim mạch khi dùng chung với clopidogrel.
Bước 3: Cân nhắc đổi thuốc kháng kết tập tiểu cầu (nếu có thể, cá thể hóa)
- Đối với những bệnh nhân nguy cơ tim mạch rất cao (ví dụ: sau đặt stent) và bắt buộc phải dùng PPI mạnh hoặc có kết quả gen đáp ứng kém với clopidogrel, bác sĩ nên cân nhắc chuyển từ clopidogrel sang Prasugrel hoặc Ticagrelor.
- Các thuốc thế hệ mới này không phụ thuộc vào enzym CYP2C19 để hoạt hóa như clopidogrel, do đó không bị ảnh hưởng hiệu lực chống huyết khối khi dùng chung với bất kỳ loại PPI nào.
3. Kết luận
Xuất huyết tiêu hóa là một trong những biến cố nghiêm trọng và thường gặp nhất ở bệnh nhân sử dụng thuốc kháng kết tập tiểu cầu, đặc biệt khi áp dụng liệu pháp kháng kết tập tiểu cầu kép. Thuốc ức chế bơm proton có vai trò quan trọng trong dự phòng xuất huyết tiêu hóa ở nhóm bệnh nhân nguy cơ cao, giúp giảm đáng kể biến cố tiêu hóa mà không làm gia tăng rõ rệt nguy cơ tim mạch khi được lựa chọn phù hợp. Trong thực hành lâm sàng, cần cá thể hóa quyết định sử dụng PPI dựa trên đánh giá đồng thời nguy cơ xuất huyết và nguy cơ huyết khối, ưu tiên các PPI ít tương tác với clopidogrel như pantoprazol hoặc rabeprazol.
TÀI LIỆU THAM KHẢO
1. Bộ Y tế (2022), Dược thư Quốc gia Việt Nam
2. Bộ Y tế (2023), Hướng dẫn Chẩn đoán và điều trị Hội chứng mạch vành mạn
3. Bộ Y tế (2024), Hướng dẫn Chẩn đoán và điều trị Đột quỵ não
4. Bộ Y tế (2020) về việc ban hành tài liệu chuyên môn Dự phòng tiên phát bệnh Tim mạch
5. Nguyễn Trung Kiên, Phạm Thành Suôl (2024), Sử dụng thuốc trong trị liệu. Nhà xuất bản Y học.
6. Brunton LL, Hilal-Dandan R, Knollmann BC, eds. Goodman & Gilman's: The Pharmacological Basis of Therapeutics. 13th ed. New York, NY: McGraw-Hill Education; 2017.
7. Robert A Byrne et al , 2023 ESC Guidelines for the management of acute coronary syndromes: Developed by the task force on the management of acute coronary syndromes of the European Society of Cardiology (ESC), European Heart Journal, Volume 44, Issue 38, 7 October 2023, Pages 3720–3826, https://doi.org/10.1093/eurheartj/ehad191
8. Gelbenegger, G., & Jilma, B. (2022). Clinical pharmacology of antiplatelet drugs. Expert review of clinical pharmacology, 15(10), 1177–1197.
9. Stanger, L., Yamaguchi, A., & Holinstat, M. (2023). Antiplatelet strategies: past, present, and future. Journal of thrombosis and haemostasis : JTH, 21(12), 3317–3328.
10. Xu, F., Zhang, Z. H., Li, L. C., Mao, K. L., & Huang, Z. Y. (2025). Bleeding in Antiplatelet Therapy: A Narrative Review of Clinical Evidence and the Roles of Pharmacists and Nurses. Reviews in cardiovascular medicine, 26(11), 45077.
11. Godier, A., Albaladejo, P., & On Perioperative Haemostasis Gihp Group, T. F. W. G. (2020). Management of Bleeding Events Associated with Antiplatelet Therapy: Evidence, Uncertainties and Pitfalls. Journal of clinical medicine, 9(7), 2318.
12. Bouget, J., Balusson, F., Viglino, D., Roy, P. M., Lacut, K., Pavageau, L., & Oger, E. (2020). Major bleeding risk and mortality associated with antiplatelet drugs in real-world clinical practice. A prospective cohort study. PloS one, 15(8), e0237022.
13. Farrokh, S., Nalleballe, K., Onteddu, S., Suarez, J. I., Bösel, J., & Shah, V. A. (2025). Bleeding Risk With Combining Antiplatelets and Anticoagulants for Secondary Stroke Prevention: A Propensity Score-Matched Analysis. Journal of the American Heart Association, 14(16), e042767.
14. Alamzaib, S. M., Maniya, M. T., Hazaveh, S., Cheema, A. A. A., Sultan, W., Qatanani, A., Mirza, M. O., Damito, S., Kumar, M., Hassan, S. A., & Khan, T. J. (2025). The risk of gastrointestinal bleeding in patients taking third-generation P2Y12 inhibitors compared with clopidogrel: systematic review and meta-analysis. Annals of medicine and surgery (2012), 87(10), 6694–6701.
15. Ejaz, M. K., Khan, M., Anthony, N., Khan, S. M., Nikalje, M., Shah, M., Anum, M., Metharayil, T. R. J., Sarooj Rasheed, A., & Mohmed Amzath, F. R. (2025). Comparative Efficacy and Safety of P2Y12 Inhibitor Monotherapy Versus Dual Antiplatelet Therapy in Patients Following Percutaneous Coronary Intervention (PCI): A Systematic Review. Cureus, 17(7), e88817.
16. Scott, S. A., Owusu Obeng, A., & Hulot, J. S. (2014). Antiplatelet drug interactions with proton pump inhibitors. Expert opinion on drug metabolism & toxicology, 10(2), 175–189.
17. Yang, H. G., & Kim, D. K. (2023). Concomitant Use of Antiplatelet Agents and Proton-Pump Inhibitors Increases the Risk of Adverse Cardiovascular Events: A Nationwide Population-Based Cohort Study Using Balanced Operational Definitions. Journal of cardiovascular development and disease, 10(6), 264.
18. Depta, J. P., & Bhatt, D. L. (2012). Antiplatelet therapy and proton pump inhibition: cause for concern?. Current opinion in cardiology, 27(6), 642–650.
19. Algabbani, A. M., Almohareb, S. N., & Alrwisan, A. A. (2025). Assessing Impact of Concomitant Use of Proton Pump Inhibitors and Clopidogrel on Incidence of Major Adverse Cardiovascular Events: A Retrospective Cohort Study. Pharmacoepidemiology and drug safety, 34(10), e70226.
20. Würtz, M., & Grove, E. L. (2017). Proton Pump Inhibitors in Cardiovascular Disease: Drug Interactions with Antiplatelet Drugs. Advances in experimental medicine and biology, 906, 325–350.
21. Huang, X., Song, J., Zhang, X., Wang, M., Ding, Y., Ji, X., Zhou, D., & Meng, R. (2025). Understanding Drug Interactions in Antiplatelet Therapy for Atherosclerotic Vascular Disease: A Systematic Review. CNS neuroscience & therapeutics, 31(2), e70258.
22. Gurbel, P. A., Tantry, U. S., & Kereiakes, D. J. (2010). Interaction between clopidogrel and proton-pump inhibitors and management strategies in patients with cardiovascular diseases. Drug, healthcare and patient safety, 2, 233–240.
ThS.DS.Nguyễn Thiên Vũ
Đơn vị Dược lâm sàng-thông tin thuốc – Khoa Dược