1. Mở đầu
Các thuốc kháng viêm không steroid (NSAIDs), bao gồm cả aspirin liều thấp, là một trong những loại thuốc được kê đơn và sử dụng phổ biến nhất trên toàn thế giới để điều trị viêm, đau khớp và bảo vệ tim mạch. Tuy nhiên, việc sử dụng chúng đi kèm với các nguy cơ tổn thương niêm mạc đường tiêu hóa nghiêm trọng, bao gồm viêm, loét, thủng và xuất huyết.
NSAIDs được xem là một nguyên nhân hàng đầu gây ra bệnh lý và tử vong do thuốc, đặc biệt ở người cao tuổi và những bệnh nhân có nhiều bệnh lý nền. Hiện nay, loét tiêu hóa do NSAIDs ở một số quốc gia đã trở thành nguyên nhân phổ biến nhất gây tổn thương dạ dày - ruột. Trong thực hành lâm sàng, thuốc ức chế bơm proton (PPI) thường được kê để dự phòng loét do NSAIDs, đặc biệt ở bệnh nhân nguy cơ cao. Tuy nhiên, tình trạng sử dụng PPI quá mức và kéo dài không cần thiết đang gia tăng, tiềm ẩn nguy cơ tác dụng phụ và chi phí điều trị.
2. Loét tiêu hóa liên quan đến kháng viêm không steroid (NSAIDs)
2.1. Cơ chế thúc đẩy loét tiêu hóa khi sử dụng NSAIDs
Cơ chế bệnh sinh ban đầu của các tổn thương dạ dày do NSAIDs được nhà khoa học Vane đề xuất vào đầu những năm 1970. Hiện nay, bệnh sinh của loét dạ dày do NSAIDs rất phức tạp và đa yếu tố, liên quan đến cả tác động toàn thân (phụ thuộc prostaglandin) và tác động tại chỗ (không phụ thuộc prostaglandin) ở cấp độ phân tử và tế bào.
- Tác động toàn thân: NSAIDs ức chế enzyme COX-1 và COX-2, làm cạn kiệt nguồn prostaglandin (đặc biệt là PGE2 và PGI2) ở dạ dày. Sự thiếu hụt prostaglandin làm giảm bài tiết chất nhầy và bicarbonate, làm giảm lưu lượng máu niêm mạc, và cản trở quá trình phục hồi, tái tạo tế bào biểu mô (angiogenesis), khiến dạ dày mất đi khả năng tự bảo vệ trước acid dịch vị với pH 1-2.
- Tác động tại chỗ: Phần lớn NSAIDs là các acid hữu cơ yếu (pKa 3-5) và ưa lipid. Trong môi trường acid của dạ dày, chúng ở dạng không ion hóa, dễ dàng khuếch tán qua lớp màng tế bào biểu mô dạ dày. Khi lọt vào bên trong tế bào chất (nơi có pH trung tính), các phân tử NSAID bị tái ion hóa, trở nên kém hòa tan trong lipid và bị “mắc kẹt” lại bên trong tế bào. Hiện tượng này gọi là bẫy ion (ion trapping).
Sự tích tụ NSAIDs trong tế bào tác động trực tiếp lên ti thể, làm mất liên kết quá trình phosphoryl hóa oxy hóa và ức chế chuỗi truyền điện tử. Điều này làm cạn kiệt ATP nội bào, gây độc tính do quá tải Canxi (Ca2+) và tạo ra hàng loạt gốc oxy hóa tự do (ROS) như superoxide. Sự cạn kiệt ATP và giải phóng gốc tự do ROS dẫn đến việc ti thể giải phóng cytochrome c, kích hoạt các chuỗi tín hiệu caspase, làm peroxy hóa lipid và cuối cùng giết chết tế bào niêm mạc thông qua con đường chết tế bào theo chương trình (apoptosis) và gây hoại tử. Bên cạnh đó, NSAIDs còn tương tác hóa học với các phospholipid ngoại bào ở màng nhầy, làm thay đổi tính kỵ nước và tính lưu động của màng, tạo ra các lỗ rỗng làm tăng tính thấm, cho phép acid khuếch tán ngược vào trong phá hủy mô.
Hình 2.1. Một số cơ chế gây tổn thương đường tiêu hóa của NSAIDs
- Một số cơ chế khác thúc đẩy loét liên quan đến NSAIDs:
+ Sự ức chế COX và tổn thương vi mạch dẫn đến việc tăng điều hòa các cytokine tiền viêm mạnh như TNF−α, IL−1β, và interleukin-8 (IL-8). Các cytokine này kích thích tế bào nội mô mạch máu và bạch cầu bộc lộ các phân tử bám vào nội mô mạch máu, gây tắc nghẽn vật lý các vi mạch. Quá trình thiếu máu cục bộ sau đó giải phóng thêm gốc tự do (ROS) và các protease phá hủy mô, đóng vai trò sống còn trong việc hình thành ổ loét ở giai đoạn sớm.
+ Nitric oxide (NO) và Hydrogen sulphide (H2S) là hai chất trung gian dạng khí giúp duy trì tính toàn vẹn niêm mạc bằng cách chống apoptosis, chống hoại tử và giãn mạch. NSAIDs làm giảm enzyme sinh NO cấu thành (cNOS) và làm tăng enzyme iNOS (do bạch cầu trung tính kích hoạt), gây rối loạn dòng máu niêm mạc. NSAIDs cũng làm giảm biểu hiện gene CSE, dẫn đến giảm sản xuất H2S – một chất bình thường giúp ngăn chặn sự bám dính của bạch cầu vào tế bào nội mô.
+ NSAIDs làm tăng hoạt động của Matrix metalloproteinase-9 (MMP-9 - enzyme phá hủy) và làm giảm MMP-2 (enzyme sửa chữa) tại mô dạ dày. Sự mất cân bằng này được điều hòa bởi các gốc ROS, làm phá vỡ quá trình tái cấu trúc chất nền ngoại bào (ECM), cản trở việc chữa lành vết thương và thúc đẩy loét tiến triển
2.2. Đặc điểm lâm sàng của loét liên quan đến sử dụng NSAIDs
Đặc điểm lâm sàng của loét tiêu hóa do thuốc kháng viêm không steroid (NSAIDs) và aspirin có những nét đặc trưng khác biệt so với các nguyên nhân gây loét thông thường, cụ thể như sau:
- Tính chất và vị trí tổn thương đa dạng
+ Tại dạ dày - tá tràng: Loét do NSAIDs thường là các ổ loét cấp tính và xuất hiện ở nhiều ổ cùng lúc. Hầu hết các ổ loét này phát triển mạnh tại vùng hang vị dạ dày, nguyên nhân là do đây là vị trí có sự sụt giảm lưu lượng máu niêm mạc nghiêm trọng nhất dưới tác động của thuốc.
+ Tại ruột non: Với sự phát triển của các kỹ thuật nội soi tiêu hóa tiến bộ, các nghiên cứu hiện nay ghi nhận NSAIDs có thể gây ra viêm, vết xước niêm mạc và loét ở ruột non với tần suất cao hơn nhiều so với dự kiến trước đây.
- Diễn biến thầm lặng và khởi phát đột ngột bằng biến chứng nặng
+ Bệnh nhân có thể gặp các triệu chứng tiêu hóa điển hình như đau vùng thượng vị (từ âm ỉ đến dữ dội), buồn nôn, nôn, chán ăn hoặc cảm giác nóng rát.
+ Một đặc điểm lâm sàng rất “thách thức” của loét do NSAIDs là thường không có triệu chứng cảnh báo trước. Trên thực tế, khoảng 15 – 20% bệnh nhân bị xuất huyết tiêu hóa do loét dạ dày tá tràng mà trước đó hoàn toàn không có tiền sử loét hay biểu hiện đau vùng thượng vị.
+ Bệnh nhân thường nhập viện cấp cứu với các biến chứng nặng, đột ngột như xuất huyết tiêu hóa (nôn ra máu đỏ tươi/máu đen, đại tiện phân đen, tụt huyết áp, mạch nhanh) hoặc thủng/tắc nghẽn dạ dày - ruột. Trên phương diện cận lâm sàng, tình trạng mất máu ẩn có thể biểu hiện qua việc sụt giảm Hemoglobin đáng kể (≥ 2 g/dL).
- Tiên lượng lâm sàng rất xấu đối với biến chứng tiêu hóa dưới
+ Trong khi tổn thương đường tiêu hóa trên có xu hướng giảm nhờ việc sử dụng kèm thuốc ức chế bơm proton (PPI), thì các biến chứng ở đường tiêu hóa dưới do NSAIDs lại đang gia tăng. Đáng chú ý, các biến chứng tại đường tiêu hóa dưới mang lại kết cục lâm sàng xấu hơn so với đường tiêu hóa trên, dẫn đến tỷ lệ tử vong cao hơn và thời gian nằm viện kéo dài hơn. Thuốc PPI cũng ít có tác dụng phòng ngừa hay ức chế được các tổn thương bệnh lý đường ruột (enteropathy) do NSAIDs gây ra.
- Mức độ biểu hiện lâm sàng phụ thuộc chặt chẽ vào các yếu tố nguy cơ của người bệnh: Ở những người sử dụng mạn tính nhưng không có yếu tố nguy cơ, tỷ lệ gặp biến cố nghiêm trọng chỉ khoảng 0,4%; tuy nhiên, rủi ro này có thể vọt lên tới 9% ở những người mang đa yếu tố nguy cơ.
2.3. Các yếu tố nguy cơ của loét liên quan đến sử dụng NSAIDs
2.3.1. Yếu tố thuộc về người bệnh
- Yếu tố di truyền (Pharmacogenomics) Sự đa hình gen chi phối quá trình chuyển hóa thuốc đóng vai trò quan trọng trong việc cá thể hóa nguy cơ quá liều NSAIDs:
+ Chuyển hóa qua enzyme CYP450: NSAIDs được chuyển hóa chủ yếu qua phân họ CYP2C ở gan (đặc biệt là CYP2C9). Các biến thể alen *2 và *3 (nhất là *3) của CYP2C9 làm giảm hoặc mất chức năng enzyme. Những người mang gen chuyển hóa kém này sẽ bị giảm thanh thải thuốc, kéo dài thời gian bán hủy và làm tăng nồng độ NSAID trong huyết tương. Do độc tính tiêu hóa của NSAID phụ thuộc vào liều, việc tích tụ thuốc này làm tăng rõ rệt nguy cơ loét và xuất huyết tiêu hóa. Bên cạnh đó, một đột biến CYP2C19*17 cũng được ghi nhận có liên quan đến bệnh loét dạ dày tá tràng do enzyme này tham gia chuyển hóa acid arachidonic; chuyển hóa quá nhanh làm suy giảm hàng rào bảo vệ niêm mạc.
Ở người châu Á, một số quần thể có tỷ lệ cao mang alen CYP2C9*3 làm tăng nguy cơ loét do tích lũy NSAID trong cơ thể. Tuy nhiên, đặc điểm đa hình của CYP2C19 lại mang đến một khía cạnh bảo vệ: người châu Á ít mang gen gây suy giảm hàng rào niêm mạc tự nhiên, đồng thời có tỷ lệ mang gen “chuyển hóa kém” PPI cao, giúp họ đáp ứng rất tốt với các liệu pháp dùng PPI để dự phòng loét do NSAID gây ra.
+ Sự đa hình của gen mã hóa enzyme COX cũng ảnh hưởng đến nguy cơ. Một số nghiên cứu sơ bộ chỉ ra rằng biến thể đa hình đơn nucleotide (SNP) rs689466 T > C trên gen COX-2 làm tăng nguy cơ xuất huyết tiêu hóa ở người dùng aspirin.
- Đặc điểm nhân trắc học và bệnh lý mắc kèm
+ Tuổi tác: Nguy cơ tăng vọt ở người cao tuổi (> 60 hoặc > 65 tuổi) do sự suy giảm chức năng sinh lý và tỷ lệ mắc đa bệnh lý cao.
+ Tiền sử loét tiêu hóa: Bệnh nhân có tiền sử bị loét (đặc biệt là loét có biến chứng xuất huyết/thủng) là nhóm có nguy cơ cao nhất bị tái phát khi dùng NSAIDs.
+ Nhiễm vi khuẩn Helicobacter pylori (H. pylori): H. pylori có tác dụng hiệp đồng với NSAIDs, làm tăng nguy cơ xuất huyết ổ loét lên gấp 1,2 lần.
+ Bệnh lý nền: Sự hiện diện của các bệnh tim mạch, đái tháo đường, suy thận (phải chạy thận nhân tạo) hoặc các tình trạng suy kiệt mạn tính đều làm tăng độ nhạy cảm của niêm mạc dạ dày đối với NSAIDs.
+ Hệ vi sinh vật đường ruột (Microbiome): Sự thay đổi hệ vi sinh vật (dysbiosis) do NSAIDs hoặc phối hợp với thuốc PPI tạo điều kiện cho vi khuẩn Gram âm phát triển, đóng vai trò quan trọng trong sinh bệnh học của tổn thương ruột non (bệnh ruột do NSAIDs).
- Mức độ tuân thủ và tương tác thuốc
+ Liều lượng và thời gian: Nguy cơ tổn thương tiêu hóa phụ thuộc tuyến tính vào liều lượng và thời gian sử dụng. Việc bệnh nhân tự ý sử dụng các thuốc NSAID không kê đơn (OTC) vượt quá liều khuyến cáo làm trầm trọng thêm vấn đề.
+ Dùng đồng thời nhiều loại thuốc: Rủi ro tăng lên rất cao khi kết hợp NSAIDs với: thuốc chống đông máu, thuốc chống kết tập tiểu cầu (kể cả Aspirin liều thấp); corticosteroid đường uống; thuốc ức chế tái hấp thu chọn lọc serotonin (SSRIs), kết hợp nhiều loại NSAID cùng lúc.
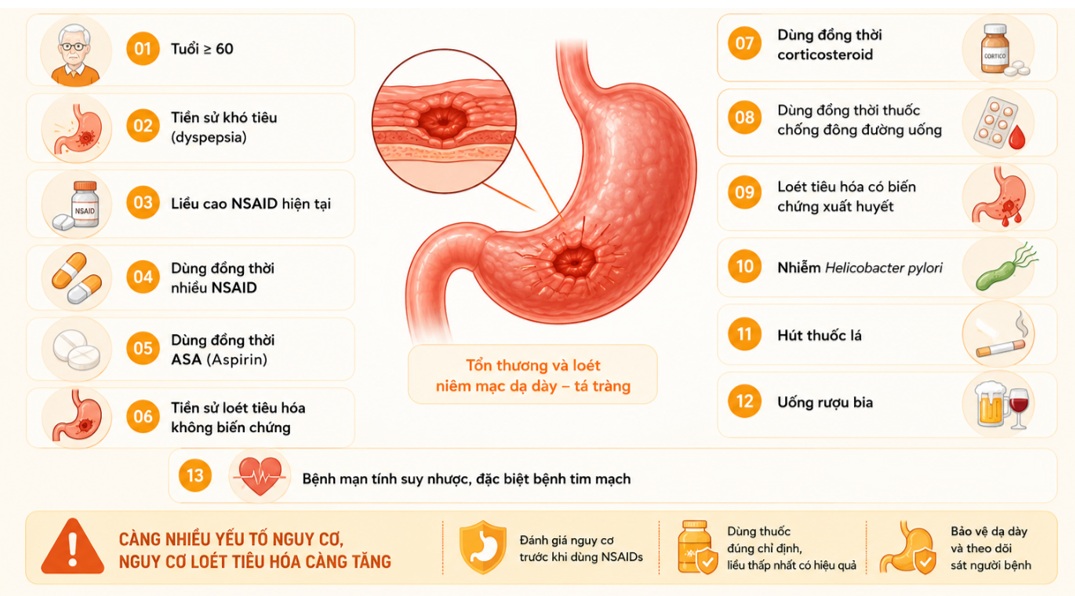
Hình 2.2. Một số yếu tố nguy cơ đồng thúc đẩy loét dạ dày ở bệnh nhân dùng NSAIDs
2.3.2. Yếu tố liên quan đến đặc tính dược lý của thuốc và dạng bào chế
- Tính chọn lọc trên enzyme Cyclooxygenase (COX)
+ NSAID không chọn lọc (ns-NSAIDs): Gây độc tính tiêu hóa cao nhất vì ức chế đồng thời cả COX-1 (enzyme chịu trách nhiệm tiết prostaglandin bảo vệ niêm mạc) và COX-2. Tổn thương lâm sàng nghiêm trọng nhất xảy ra khi cả hai đồng phân enzyme này bị ức chế.
+ Thuốc ức chế chọn lọc COX-2 (Coxibs): Giảm thiểu nguy cơ biến chứng tiêu hóa trên (loét, xuất huyết) đáng kể so với nhóm không chọn lọc, đồng thời ít gây tổn thương niêm mạc ruột non hơn.
- Tính acid và ái lực lipid: Hầu hết NSAID là các acid hữu cơ yếu (pKa 3-5) và ưa lipid. Chỉ số pKa càng thấp thì thuốc càng làm tăng tính thấm ruột và dễ gây tổn thương ruột non.
Hệ số nguy cơ giữa các hoạt chất quen thuộc nhất trên lâm sàng, thứ tự nguy cơ loét được sắp xếp tăng dần như sau: Celecoxib < Ibuprofen < Diclofenac < Meloxicam < Naproxen
- Chu trình gan - ruột: Các NSAID có chu kỳ bài tiết qua mật và tái hấp thu ở ruột (chu trình gan - ruột) gây ra sự tiếp xúc lặp đi lặp lại của niêm mạc ruột với thuốc, từ đó gây ra các tổn thương ruột non nghiêm trọng. Các mô hình động vật cho thấy NSAID nào không có chu trình này thì ít gây tổn thương ruột.
- Đường dùng và dạng bào chế
+ Đường dùng toàn thân
Nguy cơ loét tiêu hóa tương đương nhau khi dùng đường uống và đường tĩnh mạch. Việc thay đổi từ đường uống sang đường tiêm tĩnh mạch không làm loại bỏ được nguy cơ gây viêm, loét dạ dày - tá tràng. Tổn thương niêm mạc do NSAIDs bắt nguồn từ hai cơ chế: tác động tại chỗ (tiếp xúc trực tiếp làm tổn thương hàng rào niêm mạc) và tác động toàn thân (ức chế enzyme COX làm cạn kiệt prostaglandin). Khi dùng đường tĩnh mạch, mặc dù tránh được sự tiếp xúc trực tiếp ban đầu của thuốc với niêm mạc dạ dày, nhưng khi thuốc đã đi vào hệ tuần hoàn, tác động ức chế tổng hợp prostaglandin toàn thân vẫn diễn ra tương tự như đường uống. Sự thiếu hụt prostaglandin bảo vệ này mới là yếu tố thiết yếu dẫn đến sự hình thành các ổ loét trên lâm sàng. Do đó, các thuốc như indomethacin gây ra tổn thương dạ dày bất kể đường dùng là gì.
Tuy nhiên, aspirin là một trường hợp đặc biệt. Các nghiên cứu trên mô hình động vật cho thấy aspirin dường như chỉ gây loét khi được dùng qua đường uống, trong khi đường tiêm không gây tổn thương tương tự mặc dù mức độ suy giảm prostaglandin niêm mạc là như nhau. Điều này nhấn mạnh vai trò đặc biệt quan trọng của tác động gây tổn thương tại chỗ đối với cơ chế gây loét của riêng aspirin.
+ Đường dùng tại chỗ
Nguy cơ gây loet rất thấp và an toàn hơn đáng kể khi dùng đường ngoài da so với đường uống hay đường tĩnh mạch.
Các dạng bào chế NSAID dùng ngoài da (như gel bôi, miếng dán) có khả năng tạo ra nồng độ thuốc cao tại các mô đích cục bộ (như vùng cơ, khớp bị viêm) nhưng lại có nồng độ tiếp xúc toàn thân (nồng độ trong huyết tương) rất thấp. Do lượng thuốc đi vào máu không đáng kể, chúng ít gây ức chế quá trình tổng hợp prostaglandin bảo vệ dạ dày, từ đó làm giảm rõ rệt nguy cơ xảy ra các biến cố tiêu hóa nghiêm trọng so với NSAIDs đường uống.
3. Vai trò của thuốc ức chế bơm proton trong dự phòng loét do NSAIDs
3.1. Đại cương về cơ chế và vai trò của thuốc ức chế bơm proton trong dự phòng loét
Các thuốc ức chế bơm proton (proton pump inhibitors, PPIs) đầu tiên đã được đưa vào thị trường từ năm 1989, đánh dấu bước ngoặt lớn trong kiểm soát các bệnh lý mạn tính liên quan đến sự bài tiết acid dạ dày. Bản chất PPIs là những tiền chất (base yếu), không có hoạt tính và cần môi trường acid (pH thấp) để được kích hoạt.
Các thuốc PPI hiện nay (omeprazol, esomeprazol, lansoprazol, dexlansoprazol, pantoprazol, rabeprazol) đều là tiền chất cần môi trường acid để kích hoạt. Sau khi được hấp thu, PPI gắn kết cộng hóa trị (chọn lọc và không thể đảo ngược) vào các gốc cysteine của enzym H+/K+ ATPase (bơm proton) nằm trên màng tế bào thành dạ dày. Sự gắn kết này ức chế trực tiếp và hoàn toàn khâu cuối cùng của quá trình bài tiết acid dạ dày một cách phụ thuộc vào liều lượng. Vì tính chất ức chế là không thể đảo ngược, sự bài tiết acid chỉ được phục hồi khi các bơm proton mới. Về hiệu lực, các PPI có hiệu quả lâm sàng gần như tương đương nhau. Tuy nhiên, vị trí gắn cysteine và cấu trúc bào chế làm thay đổi thời gian ức chế acid. Cụ thể, dexlansoprazol ức chế dài nhất (~24 giờ) nhờ giải phóng kép, esomeprazol và rabeprazol kéo dài 16-20 giờ, trong khi omeprazol và pantoprazol duy trì khoảng 10-12 giờ.
Trên lâm sàng, việc sử dụng một số loại thuốc như thuốc kháng viêm không steroid (NSAID, bao gồm aspirin) có nguy cơ gây loét tiêu hóa. Các PPI từ lâu đã được xem là một ứng viên tiềm năng được nghiên cứu và ứng dụng để dự phòng vì chúng giúp giảm tiết acid mạnh mẽ, kéo dài và bảo vệ niêm mạc hiệu quả khi bệnh nhân sử dụng các thuốc có nguy cơ cao kéo dài. Tuy nhiên, bằng chứng ủng hộ chỉ định rộng rãi trong dự phòng loét do thuốc còn nhiều vấn đề cần thảo luận và nên được cân nhắc cá thể hóa để tránh việc sử dụng quá mức các chỉ định dự phòng, mất cân bằng hiệu quả-an toàn-chi phí khi sử dụng thuốc trên thực tế.
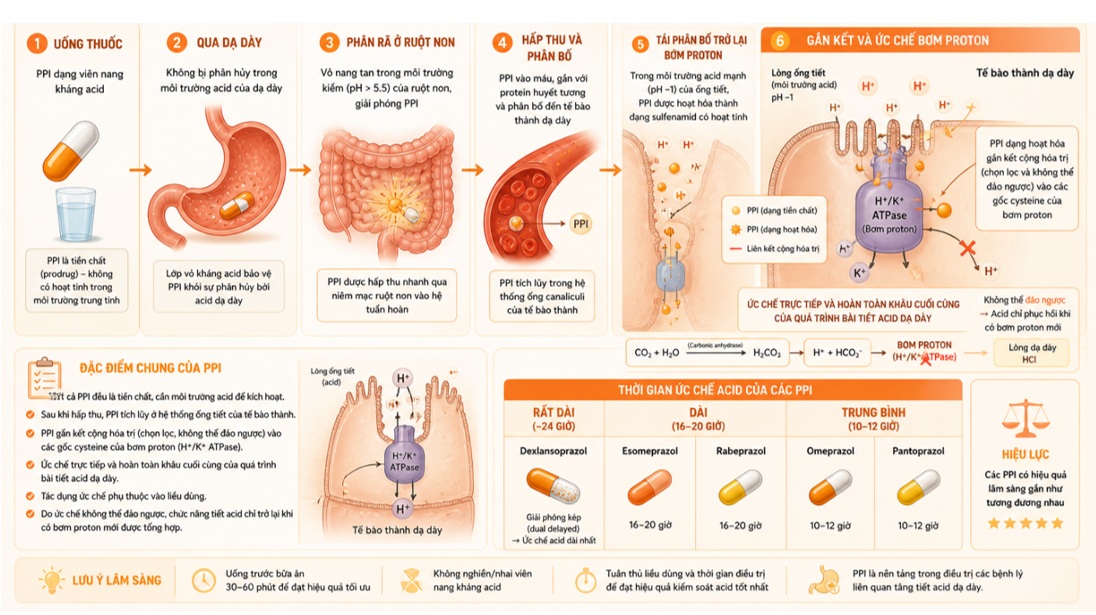
Hình 2.3. Cơ chế hoạt hóa và tác dụng của thuốc ức chế bơm proton
3.2. Hiệu quả của PPIs trong dự phòng loét do NSAIDs
Hiệu quả dự phòng loét do NSAIDs bằng thuốc ức chế bơm proton đã được công bố trên y văn qua nhiều thập niên trở lại đây. Dưới đây là một số bằng chứng tiêu biểu:
(1) Phân tích gộp và phân tích mạng lưới (networking meta-analysis) của Yang và cộng sự (2017) là một bằng chứng mạnh mẽ đánh giá hiệu quả của PPI trong dự phòng độc tính dạ dày - ruột do NSAID. Nghiên cứu bao gồm 31 thử nghiệm lâm sàng ngẫu nhiên có đối chứng (RCTs) với tổng số 12.532 bệnh nhân.
Các RCT có thời gian can thiệp trên 3 tuần; bệnh nhân có chỉ định dùng NSAID; so sánh giữa các loại PPI với nhau, hoặc PPI với placebo, thuốc kháng thụ thể H2 (H2RA), hoặc misoprostol. Kết cục đo lường phải bao gồm biến chứng loét (chảy máu, thủng, tắc nghẽn) hoặc loét phát hiện qua nội soi.
Kết quả:
+ Hiệu quả vượt trội so với placebo: PPI làm giảm có ý nghĩa nguy cơ biến chứng loét (Nguy cơ tương đối RR = 0,29; 95% CI: 0,20 - 0,42) và loét phát hiện qua nội soi (RR = 0,27; 95% CI: 0,22 - 0,33).
+ PPI hiệu quả hơn H2RA (RR = 0,26 đối với biến chứng loét) và an toàn, dễ dung nạp hơn misoprostol liều cao.
+ Chỉ số NNT (Number Needed to Treat): Để dự phòng được 1 biến chứng loét, cần điều trị bằng PPI cho 10 bệnh nhân ở nhóm nguy cơ cao, trong khi ở nhóm nguy cơ trung bình cần tới 268 bệnh nhân. Điều này cho thấy lợi ích của PPI mang lại cao nhất ở nhóm nguy cơ cao.
+ Không có sự khác biệt có ý nghĩa thống kê về hiệu quả dự phòng biến chứng loét hay loét nội soi giữa các loại PPI khác nhau (esomeprazol, omeprazol, lansoprazol, rabeprazol).
Giới hạn của nghiên cứu: Hầu hết các thử nghiệm gốc không đặt biến chứng loét làm kết cục chính nên dữ liệu biến cố khá thưa thớt. Dữ liệu về biến cố ở đường tiêu hóa dưới và ở nhóm bệnh nhân dương tính với H. pylori còn rất hạn chế. Các phân tích nhóm mang tính chất quan sát nên có thể bị ảnh hưởng bởi các yếu tố gây nhiễu.
(2) Thử nghiệm CONDOR: vai trò giới hạn của PPI trên một phần ống tiêu hóa
Đây là nghiên cứu RCT, mù đôi, phân nhóm song song đa quốc gia (32 quốc gia) với cỡ mẫu trên 4.484 bệnh nhân thoái hóa khớp hoặc viêm khớp dạng thấp cần dùng NSAID hàng ngày. Bệnh nhân ≥ 60 tuổi hoặc ≥ 18 tuổi nhưng có tiền sử loét/chảy máu tiêu hóa (nguy cơ tiêu hóa cao). Xét nghiệm âm tính với H. pylori.
Can thiệp: Nhóm dùng Celecoxib (NSAID ức chế chọn lọc COX-2) so với nhóm dùng Diclofenac (NSAID không chọn lọc) + Omeprazole (PPI) (theo dõi trong vòng 6 tháng)
Kết quả: Kết cục chính (các biến cố lâm sàng có ý nghĩa trên toàn bộ đường tiêu hóa trên và dưới) ở nhóm dùng Celecoxib là 0,9%, thấp hơn có ý nghĩa thống kê so với 3,8% ở nhóm dùng Diclofenac + Omeprazole (HR = 4,3 nghiêng về Celecoxib). Trong đó, các biến cố ghi nhận ở nhóm dùng diclofenac phối hợp omeprazol chủ yếu là tình trạng tổn thương và chảy máu rỉ rả tại ruột non gây thiếu máu nặng. Hơn 50% bệnh nhân gặp biến cố này là do bị sụt giảm Hemoglobin ≥ 2 g/dL (thiếu máu) mà không hề có dấu hiệu chảy máu đường tiêu hóa rõ ràng. Ngoài ra, hơn 60% số bệnh nhân bị thiếu máu này không tìm thấy tổn thương gây chảy máu khi nội soi dạ dày - tá tràng (OGD), cho thấy nguồn gốc xuất huyết ẩn chủ yếu đến từ các tổn thương niêm mạc ở ruột non.
Giới hạn: Nghiên cứu này gợi ý một giới hạn lớn của PPI: PPI có thể không bảo vệ được đường tiêu hóa dưới. Những bệnh nhân dùng NSAID kinh điển dù được kết hợp PPI vẫn có nguy cơ cao bị tổn thương niêm mạc (chảy máu, loét) ở ruột non và ruột già so với việc dùng NSAID ức chế chọn lọc COX-2. Hơn nữa, việc ức chế acid dạ dày bởi PPI còn có thể làm thay đổi hệ vi sinh vật ruột, làm trầm trọng thêm bệnh lý ruột do NSAID (NSAID enteropathy).
Từ kết quả của hai nghiên cứu lớn là phân tích gộp của Yang và cộng sự (2017) và thử nghiệm lâm sàng CONDOR, việc sử dụng thuốc ức chế bơm proton (PPI) dài hạn và rộng rãi để dự phòng loét do NSAIDs mang lại những lợi ích rõ rệt ở nhóm nguy cơ cao, nhưng đồng thời bộc lộ những nguy cơ và giới hạn nghiêm trọng ở đường tiêu hóa dưới. Dữ liệu y văn gợi ý rằng không nên kê đơn PPI dự phòng một cách thường quy, rộng rãi cho tất cả bệnh nhân dùng NSAIDs. PPI nên được cá thể hóa và chỉ định nghiêm ngặt cho nhóm có nguy cơ cao ở đường tiêu hóa trên. Đối với những bệnh nhân có nguy cơ cao trên toàn bộ ống tiêu hóa (đặc biệt nguy cơ xuất huyết ẩn ở ruột non), chiến lược an toàn hơn được gợi ý là sử dụng các thuốc NSAID chọn lọc COX-2 thay vì dùng NSAID kinh điển kết hợp với PPI.
3.3. Vấn đề chi phí-hiệu quả khi sử dụng PPIs trong dự phòng loét do NSAIDs
Dưới góc nhìn dược kinh tế học (chi phí - hiệu quả), việc sử dụng thuốc ức chế bơm proton (PPI) để dự phòng các biến chứng tiêu hóa do NSAIDs mang lại những kết quả khác biệt, phụ thuộc rất lớn vào nguy cơ nền của người bệnh, giá thành của loại PPI được sử dụng, và mức độ tuân thủ điều trị.
- Chi phí - hiệu quả theo phân tầng nguy cơ tiêu hóa
+ Đối với nhóm nguy cơ cao: bệnh nhân lớn tuổi, có tiền sử loét/xuất huyết, dùng kèm thuốc chống đông hoặc corticosteroid. Ở nhóm đối tượng này, chiến lược kê đơn NSAIDs kết hợp với PPI được đồng thuận là phương pháp tối ưu và mang lại hiệu quả kinh tế cao nhất.
+ Đối với nhóm nguy cơ trung bình và thấp: Các mô hình phân tích cũ thường cho rằng chỉ dùng NSAID đơn độc là giải pháp tối ưu về chi phí cho nhóm nguy cơ thấp. Tuy nhiên, một số phân tích chi phí - hữu dụng (Cost-Utility Analysis) gần đây hơn chứng minh rằng: nhờ sự sụt giảm mạnh về giá của các loại PPI generic (ví dụ: chi phí PPI chỉ khoảng €0,03/ngày), phác đồ phối hợp NSAID + PPI không chỉ đạt tiêu chuẩn chi phí - hiệu quả mà còn là một chiến lược tiết kiệm chi phí (cost-saving) so với việc chỉ dùng NSAID đơn độc và phải gánh chịu chi phí nằm viện cao hơn nếu biến chứng xảy ra.
- Giá thành của PPI quyết định tính khả thi về kinh tế
Việc lựa chọn loại PPI ảnh hưởng trực tiếp đến bài toán về chi phí. Nghiên cứu phân tích chi phí tại Hà Lan cho thấy, nếu sử dụng PPI rẻ nhất (Omeprazole generic), hệ số chi phí - hiệu quả gia tăng (ICER) chỉ ở mức khoảng €4.907 để ngăn chặn được một ca biến chứng loét nghiêm trọng. Tuy nhiên, nếu bệnh nhân sử dụng các loại PPI biệt dược đắt tiền hơn (như Esomeprazol), chi phí để ngăn chặn một biến cố sẽ tăng vọt lên tới €37.899. Mức chi phí cao này làm giảm đáng kể tính thuyết phục về mặt kinh tế của chiến lược dự phòng.
- Viên kết hợp (NSAID/PPI) so với uống các viên rời
Để giải quyết vấn đề bệnh nhân hay quên uống thuốc bảo vệ dạ dày, các dạng bào chế viên kết hợp chứa cả NSAID và PPI (ví dụ naproxen/omeprazol) trong cùng một viên đã ra đời. Dưới góc nhìn chi phí - hiệu quả:
+ Ở bệnh nhân nguy cơ trung bình: Viên kết hợp có giá thành cao, do đó chúng không đạt tiêu chuẩn chi phí - hiệu quả (ICER lên tới €35.075 cho mỗi QALY - năm sống điều chỉnh theo chất lượng) so với việc uống rời NSAID và PPI. Chúng chỉ trở nên hiệu quả về mặt kinh tế khi giá thành giảm xuống, hoặc khi mức độ tuân thủ uống thuốc rời của bệnh nhân sụt giảm xuống dưới mức 51%.
+ Ở bệnh nhân nguy cơ cao: Do xác suất biến cố lớn, lợi ích thu được từ việc đảm bảo bệnh nhân luôn dùng thuốc bảo vệ cùng NSAID tăng lên. Do đó, đối với nhóm nguy cơ cao (gấp 3 lần bình thường), viên kết hợp NSAID/PPI lại trở thành một chiến lược đạt mức chi phí - hiệu quả rất tốt (ICER giảm xuống chỉ còn khoảng €9.917 so với phác đồ uống rời).
Tóm lại, chiến lược dùng PPI để dự phòng loét do NSAIDs mang lại lợi ích kinh tế cao nhất khi bác sĩ chỉ định các loại PPI generic (giá thành thấp) ở dạng uống rời cho đa số bệnh nhân. Các dạng viên kết hợp đắt tiền hơn nên được dành riêng cho nhóm bệnh nhân có nguy cơ tiêu hóa rất cao hoặc những người được xác định là có mức độ tuân thủ điều trị kém, nhằm tối ưu hóa chi phí y tế.
3.4. Sử dụng PPIs dài hạn: các nguy cơ liên quan đến an toàn thuốc
Việc sử dụng thuốc ức chế bơm proton (PPI) dài hạn (thường gặp khi dự phòng loét dạ dày cho bệnh nhân sử dụng NSAIDs mạn tính) mang lại những lợi ích bảo vệ rõ rệt, nhưng cũng đi kèm với nhiều lo ngại về các phản ứng có hại của thuốc (adverse drug reaction, ADR). Quá trình ức chế tiết acid dịch vị mạn tính làm thay đổi sinh lý tự nhiên của dạ dày và ruột, từ đó dẫn đến nhiều nguy cơ tiềm ẩn. Dựa trên các y văn và nghiên cứu phân tích gộp, các nguy cơ liên quan đến an toàn thuốc khi dùng PPI kéo dài bao gồm:
- Rối loạn hấp thu và thiếu hụt vi chất dinh dưỡng
+ Môi trường acid của dạ dày đóng vai trò quan trọng trong việc phân giải và hấp thu các dưỡng chất. Việc giảm acid mạn tính do PPI có thể dẫn đến thiếu hụt calci, vitamin B12, thiếu sắt và thiếu máu do thiếu sắt.
+ Việc duy trì pH không acid tại dạ dày kéo dài cũng dẫn đên nguy cơ thay đổi chức năng của các protein vận chuyển magie, dẫn đến thiếu hụt magie. Tình trạng này có thể gây chuột rút, rối loạn nhịp tim hoặc co giật.
- Tổn thương xương và tăng nguy cơ gãy xương
Việc dùng PPI kéo dài có liên quan đến giảm mật độ xương và gia tăng nguy cơ gãy xương (đặc biệt là xương hông, cột sống và cổ tay). Cơ chế được cho là do hậu quả của việc giảm hấp thu Canxi, thiếu hụt Vitamin B12, hoặc do sự ức chế trực tiếp bơm proton của các tế bào hủy cốt bào (osteoclast).
- Tăng nguy cơ nhiễm khuẩn : Acid dạ dày là “hàng rào miền dịch” tự nhiên tiêu diệt các vi sinh vật nuốt vào. Khi hàng rào này suy yếu, bệnh nhân dễ bị nhiễm trùng hơn bao gồm nhiễm khuẩn đường ruột (thường do Clostridioides difficile), viêm phổi măc phải cộng đồng liên quan đến hít sặc, hội chứng vi khuẩn ruột non phát triển quá mức (SIBOd) do mất cân bằng hệ vi sinh đường ruột.
- Nguy cơ biến cố thận: Dữ liệu quan sát và tín hiệu cảnh báo an toàn từ FDA cho thấy việc dùng PPI có thể gây ra một số vấn đề trên thận bao gồm: Viêm thận kẽ cấp tính (AIN), tổn thương thận cấp (AKI), và khi sử dụng lâu dài có thể làm tăng rủi ro tiến triển thành Bệnh thận mạn tính (CKD) và bệnh thận giai đoạn cuối (ESRD). Nguyên nhân có thể do sự tích tụ các chất chuyển hóa của PPI gây ra phản ứng miễn dịch qua trung gian tế bào tại thận.
- Nguy cơ biến cố tiêu hóa và ung thư:
+ Hội chứng tăng tiết acid bù trừ: Tình trạng thiếu acid mạn tính kích thích cơ thể sản xuất nhiều hormone gastrin hơn. Tăng gastrin máu kéo dài gây ra sự tăng sản tế bào ECL (enterochromaffin-like cells), có thể hình thành các polyp tuyến phình vị (fundic gland polyps), khối u thần kinh nội tiết, và gia tăng rủi ro mắc ung thư dạ dày. Tăng gastrin cũng là nguyên nhân gây ra tăng tiết acid bù trừ (hội chứng dội ngược/rebound) khiến triệu chứng trào ngược bùng phát tồi tệ hơn khi đột ngột ngừng thuốc.
+ Tăng tổn thương ruột non do NSAID: Như đã phân tích, một nghịch lý là khi kết hợp PPI với NSAIDs kéo dài, PPI làm thay đổi hệ vi sinh vật đường ruột (dysbiosis), sự mất cân bằng này làm trầm trọng thêm các tổn thương viêm, loét, xuất huyết rỉ rả tại ruột non (NSAID-enteropathy) do NSAID gây ra.
+ Viêm đại tràng vi thể (Microscopic colitis): Nguy cơ này có thể tăng cao (lên tới hơn 3 lần) khi bệnh nhân sử dụng đồng thời cả NSAID và PPI mạn tính.
- Nguy cơ biến cố tim mạch và tương tác thuốc
+ Các PPI (đặc biệt là Omeprazole và Esomeprazole) ức chế mạnh hệ enzyme CYP2C19 ở gan, làm cản trở quá trình hoạt hóa của thuốc chống kết tập tiểu cầu Clopidogrel, qua đó có thể làm tăng nguy cơ tắc mạch ở bệnh nhân tim mạch có nhiều yếu tố nguy cơ huyết khối.
+ Một số nghiên cứu cũng cho thấy mối liên hệ (mặc dù bằng chứng còn mâu thuẫn) giữa việc dùng PPI dài hạn với rủi ro nhồi máu cơ tim hoặc đột quỵ thiếu máu não độc lập với việc dùng Clopidogrel.
- Nguy cơ biến cố thần kinh
Các bằng chứng quan sát ban đầu từng cho rằng PPI làm tăng sự tích tụ beta-amyloid gây ra sa sút trí tuệ (dementia). Tuy nhiên, các phân tích và dữ liệu ngẫu nhiên mới nhất đã bác bỏ mối liên hệ nhân quả này, đánh giá rằng nguy cơ này là không chắc chắn. Dù vậy, PPI được xác nhận là có liên quan đến việc làm tăng nguy cơ bùng phát bệnh não gan ở các bệnh nhân đã có nền xơ gan.
Tóm lại, do những tác dụng phụ nghiêm trọng khi dùng dài hạn, các hiệp hội chuyên môn khuyến cáo việc kê đơn PPI dự phòng cùng NSAIDs cần cá thể hóa, dùng liều thấp nhất có hiệu quả và thường xuyên đánh giá lại chỉ định để có kế hoạch xuống thang hoặc ngừng thuốc (deprescribing) khi không còn cần thiết, đặc biệt là khi sử dụng cho các chỉ định dự phòng.
3.5. Khuyến cáo của các hiệp hội về chỉ định PPIs trong dự phòng loét do NSAIDs
- Theo các Hướng dẫn chẩn đoán và điều trị của Bộ Y tế tại Việt Nam, việc sử dụng thuốc ức chế bơm proton (PPI) để dự phòng loét do NSAIDs/Aspirin được quy định chặt chẽ dựa trên phân tầng nguy cơ của người bệnh:
+ Đánh giá yếu tố nguy cơ:
Nguy cơ cao: Bệnh nhân trên 60-65 tuổi, cần sử dụng NSAID liều cao hoặc kéo dài, có tiền sử loét dạ dày - tá tràng (đặc biệt là loét có biến chứng), hoặc sử dụng đồng thời với aspirin, corticosteroid, thuốc chống đông máu.
Nguy cơ trung bình: Nữ giới trên 55 tuổi, có triệu chứng tiêu hóa (đau thượng vị, đầy hơi...), hút thuốc, uống rượu, nhiễm H. pylori, mắc viêm khớp dạng thấp, dinh dưỡng kém hoặc stress.
+ Chiến lược dự phòng:
Đối với bệnh nhân có nguy cơ từ trung bình đến cao, bắt buộc phải chỉ định PPI để bảo vệ dạ dày (ví dụ: Omeprazole 20mg hoặc Esomeprazole 20mg).
Nên ưu tiên sử dụng NSAID ức chế chọn lọc COX-2 kết hợp với PPI cho nhóm có nguy cơ tiêu hóa rất cao.
Trong bệnh lý tim mạch: Đối với bệnh nhân hội chứng mạch vành mạn hoặc cấp đang dùng liệu pháp chống ngưng tập tiểu cầu (đơn hoặc kép) hoặc thuốc chống đông, PPI được khuyến cáo sử dụng đồng thời nếu bệnh nhân có nguy cơ xuất huyết tiêu hóa cao.
- Khuyến cáo từ hiệp hội Tiêu hóa Hoa Kỳ (ACG):
+ Khuyến cáo dùng PPI dài hạn như một biện pháp dự phòng cho những bệnh nhân có nguy cơ cao bị xuất huyết tiêu hóa do NSAID (trên 60 tuổi, có tiền sử loét, hoặc đang dùng corticosteroid/thuốc chống đông).
+ Ở bệnh nhân bị loét xuất huyết do NSAID nhưng bắt buộc phải tiếp tục dùng NSAID, ACG khuyến cáo kết hợp PPI dùng hàng ngày cùng với một NSAID chọn lọc COX-2 ở liều thấp nhất có hiệu quả.
+ Với bệnh nhân bị loét xuất huyết do dùng aspirin liều thấp (để dự phòng tim mạch thứ phát), cần dùng PPI hàng ngày lâu dài khi dùng lại aspirin.
- Các Hiệp hội Tim mạch (ACC/AHA và ESC): Đối với bệnh nhân dùng liệu pháp kháng tiểu cầu kép (DAPT), Hội Tim mạch Châu Âu (ESC) khuyến cáo dùng PPI thường quy cho tất cả bệnh nhân, trong khi Trường môn Tim mạch/Hội Tim mạch Hoa Kỳ (ACC/AHA) khuyên chỉ dùng PPI cho những người có yếu tố nguy cơ chảy máu tiêu hóa (như tiền sử loét, dùng kèm NSAID/steroid) để tránh việc kê đơn bao vây.
4. Kết luận
Các bằng chứng hiện nay gợi ý rằng việc sử dụng thuốc ức chế bơm proton (PPI) để dự phòng loét tiêu hóa do NSAIDs không nên được áp dụng thường quy cho mọi bệnh nhân, mà cần dựa trên đánh giá nguy cơ cá thể hóa. Mặc dù PPI mang lại lợi ích rõ rệt ở nhóm nguy cơ cao như người lớn tuổi, có tiền sử loét hoặc dùng đồng thời corticosteroid, thuốc chống đông hay aspirin; lạm dụng PPI kéo dài có thể làm gia tăng nhiều biến cố bất lợi khác nhau cho người bệnh. Trong thực hành lâm sàng, bác sĩ và dược sĩ cần cân nhắc kỹ lợi ích – nguy cơ – chi phí, ưu tiên lựa chọn NSAID an toàn hơn, sử dụng PPI đúng chỉ định, đúng thời gian và thường xuyên đánh giá lại nhu cầu điều trị để tối ưu hiệu quả và an toàn cho người bệnh.
TÀI LIỆU THAM KHẢO
1. Bộ Y tế (2022), Dược thư Quốc gia Việt Nam
2. Bộ Y tế (2014), Hướng dẫn Chẩn đoán và điều trị các bệnh lý cơ xương khớp
3. Bộ Y tế (2015), Hướng dẫn Chẩn đoán và điều trị các bệnh tiêu hóa
4. Nguyễn Trung Kiên, Phạm Thành Suôl (2024), Sử dụng thuốc trong trị liệu. Nhà xuất bản Y học.
5. Brunton LL, Hilal-Dandan R, Knollmann BC, eds. Goodman & Gilman's: The Pharmacological Basis of Therapeutics. 13th ed. New York, NY: McGraw-Hill Education; 2017.
6. Ko KA, Lee DK. Nonsteroidal Anti-Inflammatory Drug-Induced Peptic Ulcer Disease. Korean J Helicobacter Up Gastrointest Res. 2025 Mar;25(1):34-41.
7. Bindu S, Mazumder S, Bandyopadhyay U. Non-steroidal anti-inflammatory drugs (NSAIDs) and organ damage: A current perspective. Biochem Pharmacol. 2020 Oct;180:114147.
8. Han H, Ro DH, Han HS, Won S. Overall compilation of adverse effects of non-steroidal anti-inflammatory drugs: a hypothesis-free systematic investigation using a nationwide cohort study. Front Pharmacol. 2025 Apr 2;16:1539328.
9. Panchal NK, Prince Sabina E. Non-steroidal anti-inflammatory drugs (NSAIDs): A current insight into its molecular mechanism eliciting organ toxicities. Food Chem Toxicol. 2023;172:113598.
10. Tawfik AG, Gomez-Lumbreras A, Del Fiol G, Kawamoto K, Trinkley KE, Reese T, Jones A, Malone DC. Nonsteroidal Anti-Inflammatory Drugs and Risk of Gastrointestinal Bleeding: A Systematic Review and Meta-Analysis. Clin Pharmacol Ther. 2026 Jan;119(1):46-62.
11. Alhammadi N, Asiri AH, Alshahrani FM, Alqahtani AY, Al Qout MM, Alnami RA, Alasiri AS, Al-Zomia AS. Gastrointestinal Complications Associated With Non-steroidal Anti-inflammatory Drug Use Among Adults: A Retrospective, Single-Center Study. Cureus. 2022 Jun 21;14(6):e26154.
12. Kei M, Uesawa Y. Comprehensive Analysis of Gastrointestinal Injury Induced by Nonsteroidal Anti-Inflammatory Drugs Using Data from FDA Adverse Event Reporting System Database. Pharmaceuticals (Basel). 2025 Aug 14;18(8):1204.
13. Srivastava H, Sehgal T, Mehta V, Berinstein J, Bishu S, Goyal MK. From pain relief to mucosal grief: A comprehensive review of NSAID enteropathy. Indian J Gastroenterol. Published online December 25, 2025.
14. Shin SJ, Noh CK, Lim SG, Lee KM, Lee KJ. Non-steroidal anti-inflammatory drug-induced enteropathy. Intest Res. 2017 Oct;15(4):446-455.
15. Shin, J. M., & Kim, N. (2013). Pharmacokinetics and pharmacodynamics of the proton pump inhibitors. Journal of neurogastroenterology and motility, 19(1), 25–35.
16. Scheiman JM. The use of proton pump inhibitors in treating and preventing NSAID-induced mucosal damage. Arthritis Res Ther. 2013;15 Suppl 3(Suppl 3):S5.
17. Yang, M., He, M., Zhao, M., Zou, B., Liu, J., Luo, L. M., Li, Q. L., He, J. H., & Lei, P. G. (2017). Proton pump inhibitors for preventing non-steroidal anti-inflammatory drug induced gastrointestinal toxicity: a systematic review. Current medical research
and opinion, 33(6), 973–980.
18. Kwok K, Tejani A. Assessing the Need for Proton Pump Inhibitors for Patients Using Long-Term Nonsteroidal Anti-inflammatory Drugs without a History of Ulcers. Can J Hosp Pharm. 2020 May-Jun;73(3):216-217. Epub 2020 Jun 1.
19. Chan, F. K., Lanas, A., Scheiman, J., Berger, M. F., Nguyen, H., & Goldstein, J. L. (2010). Celecoxib versus omeprazole and diclofenac in patients with osteoarthritis and rheumatoid arthritis (CONDOR): a randomised trial. Lancet (London, England), 376(9736), 173–179.
20. Vonkeman, H. E., Braakman-Jansen, L. M., Klok, R. M., Postma, M. J., Brouwers, J. R., & van de Laar, M. A. (2008). Incremental cost effectiveness of proton pump inhibitors for the prevention of non-steroidal anti-inflammatory drug ulcers: a pharmacoeconomic analysis linked to a case-control study. Arthritis research & therapy, 10(6), R144.
21. Maideen N. M. P. (2023). Adverse Effects Associated with Long-Term Use of Proton Pump Inhibitors. Chonnam medical journal, 59(2), 115–127.
22. Shahid, M. S., Ahmed, N., Kamal, Z., Nathaniel, L., Singla, B., Singla, S., Kumawat, S., Batool, M., Ekomwereren, O., Anika, N. N., & Sahil, M. (2025). A Systematic Review of Long-Term Use of Proton Pump Inhibitors (PPIs) in Older Adults on Polypharmacy: Do PPIs Deplete Nutrients?. Cureus, 17(8), e90888.
23. Sekar Lakshmisai, S., Bheemaneni, R. S., Nwachukwu, E. C., Nigam, A., Sakarkar, P., & Khan, S. (2025). A Systematic Review of the Adverse Effects of Long-Term Proton Pump Inhibitor Use on the Gastrointestinal System in the Adult Population. Cureus, 17(8), e90606.
24. Andrawes, M., Andrawes, W., Das, A., & Siau, K. (2025). Proton Pump Inhibitors (PPIs)-An Evidence-Based Review of Indications, Efficacy, Harms, and Deprescribing. Medicina (Kaunas, Lithuania), 61(9), 1569.
ThS.DS.Nguyễn Thiên Vũ
DSCKI.Huỳnh Ngọc Hoàn Mỹ
Đơn vị Dược lâm sàng-thông tin thuốc – Khoa Dược